CE-mærkning
Protacs sansestimulerende hjælpemidler er udviklet specifikt til at afhjælpe varige følger af en nedsat funktionsevne. Alle Protacs produkter er derfor CE-mærkede. CE-mærket betyder, at produktet lever op til de generelle sikkerheds- og sundhedskrav i forordning EU 2017/745 om medicinsk udstyr (MDR).
I EU inddeles medicinsk udstyr i 4 forskellige risikoklasser.
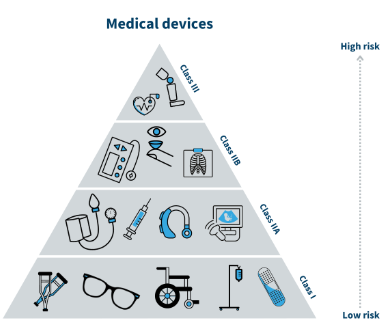
Kilde: www.laegemiddelstyrelsen.dk
Alle Protacs produkter befinder sig i klasse I, den laveste risikoklasse.
CE-mærkningsprocessen er naturligvis mest omfattende, når der er tale om højrisikoudstyr, men fælles for alle risikoklasser er, at producenten (altså her Protac) er forpligtet til at overvåge produkter på markedet, for derigennem at holde sig opdateret om, hvorvidt produkterne lever op til forventningerne, og om der er ny forskning indenfor produktområdet. Producenten er også ansvarlig for udarbejdelse og vedligeholdelse af risikoanalyse, klinisk evaluering og for at registrere sig som producent af medicinsk udstyr hos Lægemiddelstyrelsen.
Hos Protac er arbejdet med MDR en integreret del af vores kvalitetsstyringssystem. Dette betyder høj fokus på patientsikkerhed i alle processer.
Her kan du læse mere om CE-mærket og medicinsk udstyr hos Lægemiddelstyrelsen >
Ansvar for korrekt rådgivning omkring hjælpemidler
Terapeuter og sundhedspersonale har ansvaret for rådgivning omkring hjælpemidler og for at
anvendte hjælpemidler opfylder lovgivning om medicinsk udstyr.
Magasinet Ergoterapeuten har skrevet en artikel med omkring ansvar, bevilling og indkøb af hjælpemidler:
Uddrag af artiklen:
Ved indkøb af hjælpemidlet er der derudover en EU-lovgivning om medicinsk udstyr, som skal
sikre kvalitet og sikkerhed af produktet. Medicinsk udstyr vil sige produkter til at diagnosticere, forebygge, lindre, behandle sygdomme, handicap eller skader. Medicinsk udstyr må kun markedsføres, når det er CE-mærket. Med CE-mærket dokumenterer
fabrikanten produktets kvalitet, sikkerhed og ydeevne samt at produktet overholder alle
lovmæssige krav for CE-mærkning.
Her kan du læse hele artiklen >
Indberetning af hændelser
Med det ansvar som producent følger også en indberetningspligt over for eventuelle hændelser.
- Hændelser i forbindelse med brugen af Protacs produkter skal indberettes til Protac.
- Alvorlige hændelser i forbindelse med brugen af Protacs produkter skal indberettes til Lægemiddelstyrelsen samt Protac.

